SISTEM KOLOID
Tujuan Pembelajaran :
Setelah mempelajari materi ini, peserta didik diharapkan mampu:
- Menjelaskan pengertian koloid
- Menjelaskan jenis-jenis sistem koloid
- Menjelaskan sifat-sifat koloid.
- Menjelaskan proses pembuatan koloid.
- Mendeskripsikan peranan koloid di dalam kehidupan sehari-hari.
Materi:
A. Sistem Dispersi
Jika suatu zat dicampurkan dengan zat lain, akan terjadi penyebaran secara merata dari suatu zat ke dalam zat lain disebut dengan sistem dispersi. Contohnya jika tepung dimasukkan ke dalam air akan membentuk sistem dispersi. Air sebagai medium pendispersi dan tepung sebagai zat terdispersi/fase terdispersi.
Berdasarkan ukuran partikelnya, sistem dispersi dibedakan menjadi :
1. Suspensi
2. Larutan
3. Koloid
Untuk lebih memahami apakah yang dimaksud dengan suspensi, larutan dan koloid, maka perhatikan perbedaan tiga contoh campuran di bawah ini:
- Campuran antara air dengan sirup
- Campuran antara air dengan susu.
- Campuran antara air dengan pasir.
Jika kita campurkan air dengan sirup maka sirup akan terdispersi (bercampur) dengan air secara homogen (bening) Jika didiamkan, campuran itu tidak memisah dan juga tidak dapat dipisahkan dengan penyaringan biasa maupun penyaringan yang lembut (penyaringan mikro). Secara makroskopis maupun mikroskopis campuran ini tampak homogen, tidak dapat dibedakan mana yang air dan mana yang sirup. Campuran seperti inilah yang disebut larutan.
Jika kita campurkan susu (misalnya, susu instan) dengan air, ternyata susu “larut” tetapi “larutan” itu tidak bening melainkan keruh. Jika didiamkan, campuran itu tidak memisah dan juga tidak dapat dipisahkan dengan penyaringan (hasil penyaringan tetap keruh). Secara makroskopis campuran ini tampak homogen. Akan tetapi, jika diamati dengan mikroskop ultra ternyata masih dapat dibedakan partikel-partikel lemak susu yang tersebar di dalam air. Campuran seperti inilah yang disebut koloid.
Jika kita campurkan air dengan pasir maka pasir akan terdispersi (bercampur) dengan air secara heterogen dan langsung memisah antara air dengan pasir, yang keadaannya pasir akan mengendap di dasar air dan dapat dipisahkan dengan penyaringan biasa, bahkan dapat dipisahkan dengan cara dituang perlahan-lahan. Secara makroskopis campuran ini sudah tampak hetrogen, dapat dibedakan mana yang air dan mana yang pasir. Campuran seperti inilah yang disebut suspensi.
Jadi dapat disimpulkan koloid adalah suatu bentuk campuran yang keadaannya antara larutan dan suspensi. Larutan memiliki sifat homogen dan stabil. Suspensi memiliki sifat heterogen dan labil. Sedangkan koloid memiliki sifat heterogen dan stabil.
Tabel 1. Perbedaan umum antara sistem dispersi suspensi, koloid dan larutan
Perbedaan
|
Suspensi
|
Koloid
|
Larutan
|
Ukuran Partikel
|
>
100 nm
|
1-100 nm
|
< 100 nm
|
Penampilan fisik
|
Keruh, partikel terdispersi dapat
diamati langsung dengan mata
|
Keruh-jernih, partikel terdispersi
hanya dapat diamati dengan mikroskop ultra
|
Jernih, partikel terdispersi tidak
dapat diamati dengan mikroskop ultra
|
Kestabilan (jika didiamkan)
|
Mudah terpisah (mengendap)
|
Sukar terpisah (relatif stabil)
|
Tidak terpisah (sangat stabil)
|
Cara Pemisahan
|
Filtrasi (penyaringan)
|
Tidak dapat disaring
|
Tidak dapat disaring
|
B. Jenis-jenis Koloid
Jenis-jenis sistem koloid berdasarkan jenis fasa terdispersi dan medium dispersi
seperti yang tertera pada Tabel di bawah ini.
Tabel 2.
Beberapa jenis Koloid
Fase terdispersi
|
Medium Pendispersi
|
Jenis Koloid
|
Contoh
|
Padat
|
Padat
|
Sol
padat
|
Mutiara,
kaca warna
|
Padat
|
Cair
|
Sol
|
Pati
dalam air, cat, tinta
|
Padat
|
Gas
|
Aerosol
padat
|
Debu,
asap
|
Cair
|
Padat
|
Emulsi
padat
|
Keju,
mentega
|
Cair
|
Cair
|
Emulsi
|
Susu,
Mayones, santan
|
Cair
|
Gas
|
Aerosol
cair
|
Awan,
kabut
|
Gas
|
Padat
|
Buih
padat
|
Batu
apung, karet busa
|
Gas
|
Cair
|
Buih
|
Krim
kocok, busa sabun
|
C. Sifat-sifat Koloid
1.
Efek
tyndall
Efek tindal yaitu efek penghamburan
cahaya oleh partikel koloid. Efek tyndall ini ditemukan oleh John Tyndall
(1820-1893), seorang ahli fisika Inggris. Oleh karena itu sifat itu disebut
efek tyndall. Efek Tyndall adalah efek yang terjadi jika suatu larutan terkena
sinar. Pada saat larutan sejati (gambar kiri) disinari dengan cahaya, maka
larutan tersebut tidak akan menghamburkan cahaya, sedangkan pada sistem koloid
(gambar kanan), cahaya akan dihamburkan.
Hal itu terjadi karena
partikel-partikel koloid mempunyai partikel-partikel yang relatif besar untuk
dapat menghamburkan sinar tersebut. Sebaliknya, pada larutan sejati,
partikel-partikelnya relatif kecil sehingga hamburan yang terjadi hanya sedikit
dan sangat sulit diamati.
Gambar 1. Efek Tyndall
Gambar hamburan cahaya oleh air santan
kelapa (koloid) dan larutan gula yang bukan koloid
Contoh efek tyndall dalam kehidupan
sehari-hari:
a.
Jika
sinar matahari masuk melalui celah ke dalam ruangan, pada sinar tersebut
terlihat debu-debu beterbangan.
b. Pada
malam hari pada jalan yang berdebu, berkas nyala lampu mobil dapat terlihat
dengan jelas, karena disebarkannya
cahaya lampu oleh partikel-partikel debu yang disinarinya,
c. Sorot lampu proyektor dalam gedung bioskop yang
berasap,
d. Berkas sinar matahari melalui celah daun pohon-
pohon pada pagi hari yang berkabut.
2.
Gerak
brown
Gerak
brown adalah gerak tidak beraturan atau gerak acak atau gerak zig-zag partikel
koloid. Hal ini terjadi karena adanya benturan tidak teratur dari partikel
koloid dengan medium pendispersi. Dengan adanya gerak Brown ini maka partikel
koloid terhindar dari pengendapan karena terus-menerus bergerak, sehingga
koloid menjadi stabil. Gerak zig-zag partikel koloid disebut gerak Brown,
sesuai dengan nama penemunya Robert Brown seorang ahli biologi
berkebangsaan Inggris.
Gambar
2. Robert Brown dan gerak brown.
3.
Adsorpsi
Adsorpsi yaitu penyerapan muatan oleh permukaan
partikel koloid. Contoh:
Koloid Fe(OH)3 bermuatan positif karena permukaannya
menyerap ion H+. Sedangkan koloid As2S3
bermuatan negatit karena permukaannya menyerap ion S2-. Perhatikan gambar.


Gambar
3. Adsorbsi pada permukaan koloid
Adsorbsi berbeda dengan absorbsi,
absorpsi penyerapan yg terjadi di seluruh bagian. Sifat adsorpsi partikel
koloid dalam kehidupan sehari digunakan pada proses-proses berikut:
a.
Pemutihan gula tebu, zat
warna pada tebu diadsopsi sehingga putih bersih
b.
Pengobatan sakit perut dengan norit. Obat norit bahan dasarnya adalah karbon aktif, di dalam usus besar membentuk
koloid yang dapat
mengadsopsi gas atau zat warna.
c.
Penjernihan air, menambahkan tawas dapat mengadsorpsi zat warna pada air kotor.
4.
Elektroforesis
 Peristiwa bergeraknya partikel koloid
dalam medan listrik disebut dengan elektroforesis. . Partikel koloid yang bermuatan negatif akan menuju
ke
anoda (elektroda positif) dan sebaliknya partikel koloid yang bermuatan posistif akan menuju katoda. Gejala ini disebut
elektroforesis. Pada peristiwa elektroforesis, partikel-partikel
koloid akan
dinetralkan
muatannya dan
digumpalkan di bawah elektroda.
Peristiwa bergeraknya partikel koloid
dalam medan listrik disebut dengan elektroforesis. . Partikel koloid yang bermuatan negatif akan menuju
ke
anoda (elektroda positif) dan sebaliknya partikel koloid yang bermuatan posistif akan menuju katoda. Gejala ini disebut
elektroforesis. Pada peristiwa elektroforesis, partikel-partikel
koloid akan
dinetralkan
muatannya dan
digumpalkan di bawah elektroda.
Proses elektroforesis ini digunakan untuk menentukan muatan koloid, apakah positif atau negatif.
Selain itu dimanfaatkan dalam proses pemisahan potongan-potongan gen pada
proses bioteknologi dan penyaring debu pabrik pada cerobong asap yang disebut
pengendap Cottrel.
5. Koagulasi
Koagulasi adalah penggumpalan partikel koloid. Koagulasi dapat dilakukan
dengan cara
mekanik dan kimia yaitu :
a. Mekanik
: pemanasan atau pendinginan
b. Kimia :
1) Pencampuran koloid yang berbeda muatan.
Contoh :
sol Fe(OH)3 yang bermuatan positif ditambah sol As2S3 yang
bermuatan negatif, maka akan terjadi koagulasi.
Gambar 6. Pencampuran
koloid berbeda muatan
2) Penambahan elektrolit.
Contoh:
a)
Pengolahan karet dari bahan mentahnya ( lateks ) dengan
koagulan berupa asam format.
b)
Proses penjernihan air dengan menambahkan tawas.
Tawas aluminium sulfat (mengandung ion Al3+) dapat digunakan untuk
menggumpalkan lumpur koloid atau sol tanah liat dalam air (yang bermuatan
negatif).
c)
Proses terbentuknya delta di muara sungai. Terjadi
karena koloid tanah liat dalam air sungai mengalami koagulasi ketika bercampur
dengan elektrolit dalam air laut.
d)
Asap atau debu pabrik dapat digumpalkan dengan alat
koagulasi listrik (pesawat Cottrel ). Metode ini dikembangkan
oleh Frederick Cottrel ( 1877 - 1948
).
e)
Proses yang dilakukan oleh ion Al3+ atau
Fe3+ pada penetralan partikel
albuminoid yang terdapat dalam darah, mengakibatkan terjadinya koagulasi
sehingga dapat menutupi luka.
6.
Kestabilan Koloid
a.
Menghilangkan
muatan koloid
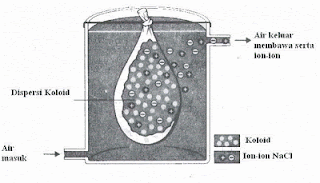
Proses
penghilangan muatan koloid dilakukan dengan proses dialisis. Dialisis adalah
proses menghilangkan muatan koloid dengan cara memasukkan ke dalam membran
semipermeabel. Membran ini mempunyai pori-pori yang mampu ditembus ion, tetapi
tidak mampu ditembus koloid
Gambar 7. Kantong
semipermeabel
Salah
satu pemanfaatan dialisis adalah proses cuci darah (hemodialisis). Pada proses hemodialisis, darah kotor dari
pasien dilewatkan dalam pipa – pipa yang terbuat dari membran semipermeabel.
Selama darah berjalan, pipa semipermeabel tersebut dialiri cairan (biasanya
plasma darah) sehingga ion – ion dalam darah kotor tadi akan terbawa pada
aliran plasma darah yang berfungsi sebagai pencuci.
b.
Penambahan
stabilisator koloid
Penambahan
suatu zat ke dalam suatu sistem koloid dapat meningkatkan kestabilan koloid,
misalnya emulgator dan koloid pelindung. • Emulgator adalah zat yang
ditambahkan ke dalam suatu emulsi (koloid cair dalam cair atau cair dalam
padat) dengan tujuan menjaga koloid agar tidak mudah terpisah. Sebagai contoh
penambahan sabun ke dalam campuran minyak dan air serta penambahan amonia dalam
pembuatan emulsi pada kertas film. • Koloid pelindung adalah koloid yang
ditambahkan ke dalam sistem koloid agar menjadi stabil. Sebagai contoh
penambahan gelatin pada pembuatan es krim agar es krim tidak cepat memisah
serta penambahan gum arab dalam pembuatan semir.
7.
Koloid Liofil dan Koloid Liofob
Koloid liofil adalah koloid yang fase terdispersinya
suka menarik medium pendispersinya. Peristiwa ini disebabkan gaya tarik antara
partikel – partikel terdispersi dengan medium pendispersinya kuat. Koloid
liofob adalah sistem koloid yang fase terdispersinya tidak suka menarik medium
pendispersinya. Jika medium pendispersinya air, koloid liofil disebut juga
sebagai koloid hidrofil, sedangkan koloid liofob disebut sebagai koloid
hidrofob.
Tabel 3. Perbandingan liofil dan liofob
Pemanfaatan sifat hidrofob dan hidrofil adalah pada
penggunaan deterjen dalam proses pencucian pakaian.
D. Pembuatan Koloid
Terdapat dua
cara pembuatan koloid yaitu cara kondensasi dan cara dispersi.
1. Cara
Dispersi
Cara dispersi adalah memperkecil
partikel. Cara ini melibatkan pengubahan ukuran partikel besar (misalnya
suspensi atau padatan) menjadi ukuran partikel koloid.
a)
Dispersi langsung (mekanik)
Cara ini
dilakukan dengan memperkecil zat terdispersi sebelum didispersikan ke dalam
medium pendispersi. Ukuran partikel dapat diperkecil dengan menggiling atau
menggerus partikel sampai ukuran tertentu. Alat yang digunakan untuk cara ini
biasa disebut penggilingan koloid, yang biasa digunakan dalam:
Ø
Industri
makanan untuk membuat jus buah, selai, krim, es krim,dsb.
Ø
Industri
kimia rumah tangga untuk membuat pasta gigi, semir sepatu, deterjen, dsb.
Ø
Industri
kimia untuk membuat pelumas padat, cat dan zat pewarna.
Ø
Industri-industri
lainnya seperti industri plastik, farmasi, tekstil, dan kertas.
b)
Homogenisasi
Pembuatan susu kental manis yang bebas
kasein dilakukan dengan mencampurkan serbuk susu skim ke dalam air di dalam
mesin homogenisasi sehingga partikel-partikel susu berubah menjadi seukuran
partikel koloid.
c) Peptisasi
Proses peptisasi dilakukan dengan cara
memecah partikel-partikel besar, misalnya suspensi, gumpalan, atau endapan
dengan menambahkan zat pemecah tertentu. Zat pemecah tersebut dapat berupa
elektrolit khususnya yang mengandung ion sejenis ataupun pelarut tertentu.
Contoh:
Ø
Agar-agar
dipeptisasi oleh air, karet oleh bensin
Ø
Endapan
NiS dipeptisasi oleh H2S, endapan Al(OH)3 oleh AlCl3
Ø
Sol
Fe(OH)3 diperoleh dengan mengaduk endapan Fe(OH)3 yang baru
terbentuk dengan sedikit FeCl3. Sol Fe(OH)3 kemudian
dikelilingi Fe+3 sehingga bermuatan positif
Ø
Beberapa
zat mudah terdispersi dalam pelarut tertentu dan membnetuk sistem koloid.
Contohnya: gelatin dalam air.
d) Busur
Bredig
Busur
Bredig adalah suatu alat yang khusus digunakan untuk membentuk koloid logam.
Proses ini dilakukan dengan cara meletakkan logam yang akan dikoloidkan pada
kedua ujung elektrode dan kemudian diberi arus listrik yang cukup kuat sehingga
terjadi loncatan bunga api listrik. Suhu tinggi akibat adanya loncatan bunga
api listrik mengakibatkan logam akan menguap dan selanjutnya terdispersi ke
dalam air membentuk suatu koloid logam.
Gambar 8. Cara busur listrik Bredig
2. Cara
Kondensasi
Cara kondensasi dilakukan dengan
mengubah suatu larutan menjadi koloid. Proses ini umumnya melibatkan
reaksi-reaksi kimia yang menghasilkan zat yang menjadi partikel-partikel
terdispersi.
a)
Reaksi
hidrolisis
Reaksi ini
umumnya digunakan untuk membuat koloid-koloid basa dari suatu garam yang
dihidrolisis (direaksikan dengan air). Contoh : Pembuatan sol Fe(OH)3 dengan cara memanaskan larutan
FeCl3.
FeCl3(aq)
+ 3H2O(l) → Fe(OH)3 (koloid) + 3HCl(aq)
b)
Reaksi
redoks
Reaksi
yang melibatkan perubahan bilangan oksidasi. Koloid yang terjadi merupakan
hasil oksidasi atau reduksi. Contoh : Pembuatan sol belerang dengan cara
mengalirkan gas H2S ke dalam larutan SO2.
2H2S(g)
+ SO2(aq) → 3S(s) + 2H2O
c)
Pertukaran
ion
Reaksi pertukaran ion umumnya dilakukan
untuk membuat koloid dari zat-zat yang sukar larut (endapan) yang dihasilkan
pada reaksi kimia. Contoh : Pembuatan sol As2S3 dengan mengalirkan gas H2S ke
dalam larutan As2S3.
3H2S(g) + As2O3(aq) -> As2S3(s) +
3H2O(l)
Selain dengan cara-cara tadi, koloid
ada yang terbentuk secara alamiah, misalnya lumpur, getah karet, dan getah
pohon nangka.










Tidak ada komentar:
Posting Komentar